中志集团重大突破!揭示硒介导实体瘤免疫调控新机制,成果登IF3.8国际权威期刊
2026/4/3
近日,安徽中志集团旗下子公司(安徽中志科技有限公司)与合肥师范学院化学与制药工程学院联合在国际权威期刊《Food Science & Nutrition》(IF=3.8,JCR Q2)发表了题为"Metabolic Functions and Mechanisms of Selenium, Selenocysteine, and GPX4 Mediated Immune Regulation Through Autophagy in Solid Tumors"的重要研究成果。
![]()
该研究由公司技术团队与合肥师范学院杨亮副教授、23级本科生江雨等共同完成,系统阐述了硒代谢关键蛋白GPX4通过自噬途径调控实体肿瘤铁死亡和免疫应答的分子机制。
《Food Science & Nutrition》
Food Science & Nutrition创刊于2013年,专注于食品科学与营养学领域的基础与应用研究。期刊由Wiley-Blackwell出版,该机构是国际顶尖学术出版集团之一,在科学、技术、医学等领域拥有深厚的学术积累和全球声誉,依托优质的出版资源与严谨的学术审核体系,该期刊刊发的文章始终保有极高的被引用率和同行认可度,其研究成果也具有较高的参考价值和传播力。
研究背景及意义
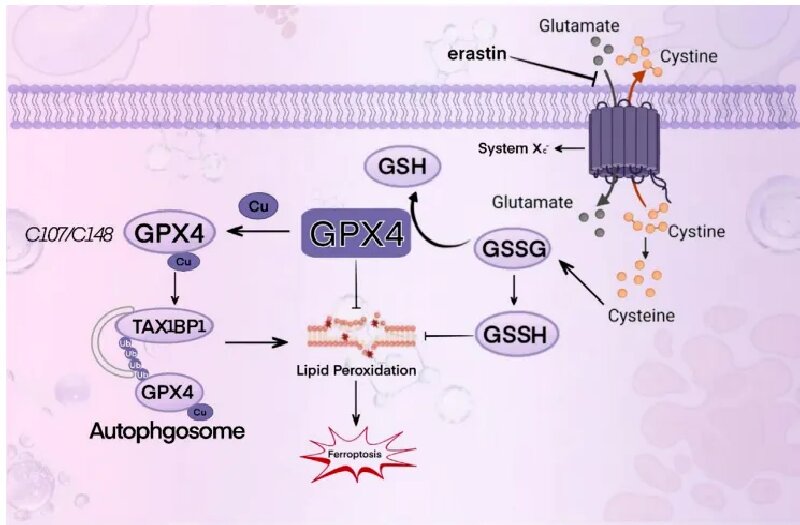
硒作为人体必需的微量元素,在抗氧化、免疫调节等方面发挥关键作用。在实体肿瘤微环境中,癌细胞通过硒代谢途径上调GPX4表达,建立针对铁死亡的防御机制,从而产生治疗抵抗。本研究创新性地揭示了自噬受体TAX1BP1/SQSTM1介导的GPX4降解途径,为克服肿瘤耐药提供了新的理论依据。
![]()
在本综述中,全面且深入地剖析了硒代谢所产生的硒蛋白在免疫细胞调控相关免疫疾病方面所发挥的作用,并详细阐述了GPX4在自噬介导的免疫调节作用下,针对实体肿瘤中铁死亡所产生的关联效应。
核心发现与机制解析
●硒代谢的双向调控作用
研究团队发现,癌细胞通过SLC7A11转运体高效摄取硒元素,经SEPHS2酶介导的代谢途径合成GPX4。GPX4作为关键抗氧化酶,可清除脂质过氧化物,维持癌细胞存活。然而,这种防御机制也成为了新的治疗靶点。
研究指出,铜离子(Cu²⁺)和铁死亡诱导剂erastin可通过激活自噬途径,分别促使TAX1BP1和SQSTM1受体识别并降解GPX4。这一过程显著增强了癌细胞对铁死亡的敏感性,尤其在乳腺癌、结直肠癌等实体肿瘤中表现突出。
●免疫调节的协同效应
研究还发现,GPX4降解触发的铁死亡可重塑肿瘤免疫微环境。一方面促进CD8⁺T细胞浸润,另一方面通过调控IL-1β等炎症因子分泌,打破免疫耐受状态,为免疫治疗联合策略提供了新思路。研究采用多组学整合分析方法,通过对265篇核心文献的系统综述,首次构建了"硒代谢-GPX4-自噬-免疫调节"的全新信号网络。特别值得关注的是,团队发现跨膜蛋白TMEM164在自噬依赖性铁死亡中起关键桥梁作用,这为靶向药物开发提供了新靶点。
产学研合作价值
本研究体现了安徽中志科技有限公司在硒化合物应用研发方面的技术优势,结合合肥师范学院在基础研究领域的深厚积累,不仅揭示了硒代谢在肿瘤治疗中的新功能,还为开发基于硒纳米颗粒的特医食品提供了理论指导。该研究成果也为实体肿瘤的治疗提供了新范式:通过调控硒代谢通路可精准诱导癌细胞铁死亡,同时激活抗肿瘤免疫应答。这种"一石二鸟"的治疗策略,有望解决当前肿瘤治疗中的耐药难题,具有重要的临床转化价值。
安徽中志集团对旗下子公司安徽中志科技有限公司与合肥师范学院联合取得的这一重要研究成果倍感珍视,并积极推动成果在集团内部及行业领域的共享与转化。集团深知硒代谢相关研究在肿瘤治疗领域的巨大潜力,将以该成果为重要契机,充分整合内外资源,大力推动硒化合物在肿瘤营养治疗领域的创新应用探索,为提升肿瘤治疗水平、守护人类健康事业贡献力量。
![]()
![]()
![]()
安徽中志土壤研究院集团有限公司 版权所有 皖ICP备18022639号-1 免责声明